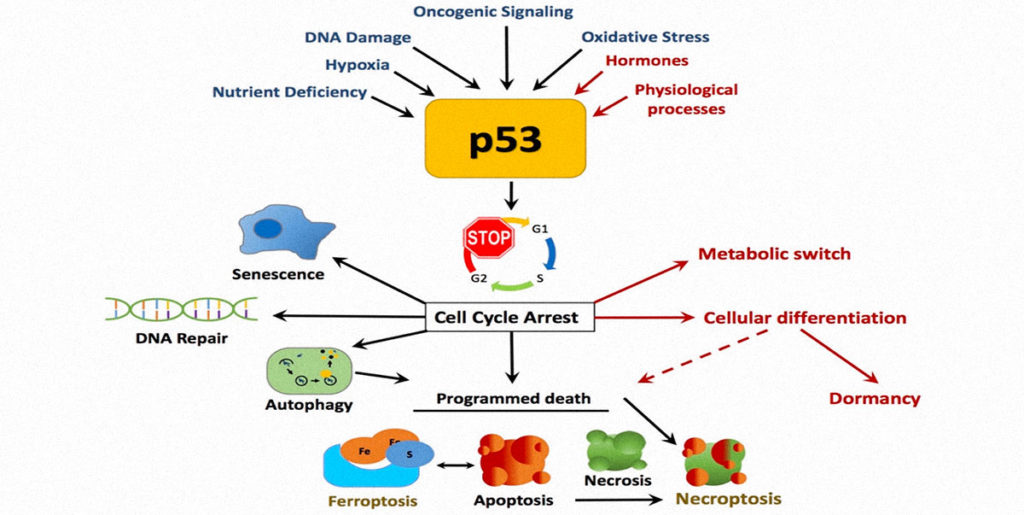
La P53, anche conosciuta come proteina tumorale 53 (gene TP53), è un fattore di trascrizione che regola il ciclo cellulare e ricopre la funzione di soppressore tumorale. La sua funzione è particolarmente importante negli organismi pluricellulari per sopprimere i tumori nascenti.
Riportiamo l’ultima pubblicazione al riguardo:
Il mutante p53 induce la tubulo-vescicolazione del Golgi guidando un secretoma prometastatico
Astratto
TP53mutazioni missenso che portano all’espressione di oncoproteine p53 mutanti sono eventi driver frequenti durante la tumorigenesi. I mutanti p53 promuovono la crescita, le metastasi e la chemioresistenza del tumore influenzando le vie e le funzioni cellulari fondamentali. Qui, dimostriamo che i mutanti p53 modificano la struttura e la funzione dell’apparato di Golgi, culminando nell’aumentato rilascio di un secretoma pro-maligno da parte delle cellule tumorali e dei fibroblasti primari da pazienti con sindrome da predisposizione al cancro Li-Fraumeni. Meccanicamente, interagendo con il fattore reattivo all’ipossia HIF1α, il mutante p53 induce l’espressione di miR-30d, che a sua volta provoca la tubulo-vescicolazione dell’apparato del Golgi, portando a un aumento del traffico vescicolare e della secrezione.
introduzione
Il crosstalk delle cellule tumorali con il microambiente tumorale (TME) gioca un ruolo cruciale nella crescita e nella progressione del tumore. I tumori riprogrammano il loro fenotipo secretorio per modellare un microambiente permissivo, supportando l’invasione locale e la colonizzazione delle nicchie metastatiche 1 . Ciò comporta il rilascio di fattori solubili che stimolano l’angiogenesi e il reclutamento di popolazioni di cellule stromali e immunitarie 2 , 3 , nonché la deposizione e il rimodellamento della matrice extracellulare (ECM) per sostenere la meccano-stimolazione 4 .
Sebbene siano state caratterizzate molte molecole e tipi di cellule coinvolti nella comunicazione tumore-stroma, i fattori responsabili della riprogrammazione dell’attività secretoria delle cellule tumorali rimangono poco conosciuti. Diversi rapporti indicano che le cellule tumorali adattano il loro meccanismo secretorio, vale a dire il reticolo endoplasmatico (ER) e l’apparato di Golgi (GA), per affrontare una maggiore traduzione e secrezione proteica 5 , 6 . Inoltre, prove recenti suggeriscono che le alterazioni del GA e l’ottimizzazione del traffico vescicolare conferiscono alle cellule tumorali fenotipi aggressivi e metastatici 7 , 8 . Il modo in cui queste alterazioni si relazionano alla segnalazione oncogena è, tuttavia, in gran parte sconosciuto.
Le mutazioni missenso nel gene TP53 , che causano l’espressione delle proteine mutanti p53 (mut-p53), sono tra le alterazioni genetiche più frequenti nei tumori umani e sono associate alla sindrome di Li-Fraumeni, una rara predisposizione familiare al cancro 9 , 10 . Mut-p53 perde le funzioni di soppressione del tumore e può acquisire proprietà che gli consentono di ricablare il trascrittoma e il proteoma della cellula, promuovendo la crescita del tumore, la chemioresistenza e le metastasi 11 , 12 , 13 . Mut-p53 viene spesso stabilizzato e attivato da segnali meccanici come la rigidità ECM 14, e impatta sulla diafonia tra cellule cancerose e stroma regolando l’espressione di citochine e chemochine, inducendo così la migrazione e l’invasione delle cellule tumorali in modo paracrino 15 . Tuttavia, l’impatto di mut-p53 sul meccanismo secretorio e gli effetti del secretoma dipendente da mut-p53 sulla TME nei siti locali e distali rimangono scarsamente definiti. È stato dimostrato che i mutanti missenso di p53 regolano diversi miRNA 16 , 17 , alcuni dei quali sono secreti e concorrono all’evoluzione maligna per effetti a lungo raggio 18 .
In questo lavoro indaghiamo come mut-p53 modifichi i processi cellulari alterando la comunicazione delle cellule cancerose con il loro microambiente. Come potenziali mediatori di questa attività ci siamo concentrati sui miRNA regolati da mut-p53, una classe di molecole in grado di modulare a più livelli interi processi cellulari. Abbiamo scoperto che mut-p53, attraverso il suo target miR-30d, controlla il traffico secretorio delle cellule tumorali provocando la tubulo-vescicolazione del GA. Ciò aumenta il rilascio di un secretoma pro-maligno, che ha un impatto sulla TME, favorendo la crescita del tumore e la colonizzazione metastatica.
risultati
MicroRNA-30d è un nuovo bersaglio del mutante p53
Per identificare mut-p53 miRNA bersaglio, abbiamo silenziato mut-p53 R280K in MDA-MB-231 cellule di cancro al seno di RNAi e vigilato i livelli di un gruppo di miRNA, precedentemente trovato sovraespresso in tipi di tumori solidi ad alta frequenza di missense TP53 mutazioni 19 , 20 (Figura supplementare 1a ). Tra i miRNA la cui espressione è stata ridotta al knockdown di mut-p53 abbiamo identificato miR-30d, precedentemente segnalato per esercitare attività oncogeniche 21 , 22 , 23 , 24 , 25 . L’espressione di miR-30d è stata significativamente ridotta al knockdown di mut-p53, mentre la reintroduzione di p53 R280K insensibile a siRNAaumentato (Fig. 1a ). Effetti simili sono stati osservati in linee cellulari che ospitano diverse varianti mut-p53, dalla mammella (MD-MB-468 / p53 R273H , SK-BR-3 / p53 R175H e SUM-159PT / p53 R158insS ) (Fig. 1b ), prostata , colon, fegato e cancro dell’ovaio (DU 145 / p53 P223L, V274F , HT-29 / p53 R273H , Mahlavu / p53 R249S , TOV-112D / p53 R175H , Figura supplementare 1b ). Il silenziamento della p53 wild-type non ha avuto effetto sui livelli di miR-30d nelle cellule tumorali HBL100 e MCF-7, così come nelle cellule epiteliali mammarie normali MCF10A (Fig. 1c , Figura supplementare 1c). Al contrario, l’espressione ectopica delle varianti mut-p53 R175H, R273H e R280K nelle cellule MCF10A, stabilmente silenziate per wt-p53, ha aumentato l’espressione di miR-30d (Fig. 1c ). Confermando la dipendenza da mut-p53, i livelli di miR-30d sono stati ridotti dopo il trattamento delle cellule MDA-MB-231 con l’agente inattivante mut-p53 APR-246 / PRIMA-1MET, in grado di ripristinare la funzione wt-p53 26 (Figura 1d supplementare ) . Inoltre, il disaccoppiamento del segnale meccanico mediante coltura di cellule su matrice morbida o trattamento con l’inibitore della miosina II Blebbistatin o l’inibitore HDAC6 sulforafano ha ridotto significativamente i livelli di mut-p53 e l’espressione di miR-30d, simile al silenziamento di mut-p53 (Figura complementare. 1d, e ).
Mut-p53 induce l’espressione di miR-30d attraverso HIF1α
Successivamente abbiamo studiato il meccanismo della regolazione di miR-30d da parte di mut-p53. L’analisi qPCR ha indicato che mut-p53 modula i livelli di miR-30d primario (pri-miR-30d), precursore (pre-miR-30d) e maturo in misura simile (Fig. 1a, d ), suggerendo che controlla miR -30d trascrizione. Le regioni regolatorie genomiche di MIR30D non sono caratterizzate, tuttavia, la regione che circonda il sito di inizio della trascrizione 27 , 28 mostrava segni di cromatina promotore attivo 29 (Figura complementare. 1f ), è stata identificata come bersaglio di mut-p53 mediante sequenziamento ChIP 30 e è vincolato dai fattori di ipossia HIF1α e HIF2α in caso di ipossia 31. Questo ci ha spinto a verificare se mut-p53 potesse regolare la trascrizione di miR-30d attraverso HIF. Come mostrato nella Figura 1g supplementare , l’espressione ectopica di HIF1α ha aumentato i livelli di miR-30d, mentre la sua deplezione ha downregolato sia il precursore che il miR-30d maturo nelle cellule MDA-MB-231 (Figura supplementare 1h ). Inoltre, silenziando HIF1α o mut-p53 ha impedito l’induzione di miR-30d da ipossia (2% pO 2 ) (Fig. 1e ). Poiché l’attività trascrizionale di mut-p53 cambia allo spostamento delle cellule dalla coltura 2D a quella 3D 32 , abbiamo confermato che l’induzione di miR-30d da ipossia dipendeva da mut-p53 anche quando si coltivano cellule MDA-MB-231 in 3D (Figura 1i supplementare ).
Successivamente, abbiamo verificato se mut-p53 e HIF1α interagiscono: i saggi di legatura di prossimità (PLA) hanno rivelato complessi nucleari tra mut-p53 e HIF1α, la cui formazione è stata migliorata a bassa pressione di ossigeno e al trattamento ipossia-mimetico con CoCl 2 (Fig. 1f ). Risultati simili sono stati ottenuti mediante co-immunoprecipitazione di proteine mut-p53 e HIF1α da lisati di cellule MDA-MB-231 cresciute sotto diversa pressione di ossigeno (Figura complementare 1j ), nonché da cellule MDA-MB-468, entrambe in normossia e dopo trattamento ipossia-mimetico (Figura complementare 1k ).
Coerentemente, l’analisi di un set di dati 33 sull’espressione genica del cancro al seno ha evidenziato una correlazione tra mutazioni missenso di TP53 e un’elevata attività di HIF1α (Figura 1l supplementare ). Inoltre, un’elevata espressione di miR-30d era associata alla mutazione di TP53 e ad alti livelli di HIF1α nei set di dati di espressione genica del cancro (Figura complementare 1m, n ).
Infine, per verificare se mut-p53 e HIF1α attivano cooperativamente il promotore MIR30D , abbiamo eseguito esperimenti ChIP in cellule MDA-MB-231. In normossia abbiamo osservato il legame di mut-p53 al promotore di MIR30D , che è stato ulteriormente migliorato in ipossia in modo dipendente da HIF1α (Fig. 1g ). D’altra parte, mut-p53 era richiesto per il reclutamento efficiente di HIF1α al promotore MIR30D in condizioni di normossia e ipossia (Fig. 1h ) e per l’acetilazione dell’istone H3 Lisina 9 (H3K9ac) (Fig. 1i ), che si verifica durante l’ipossia indotta attivazione trascrizionale 34 in questa regione genomica.
Questi risultati suggeriscono che nelle cellule tumorali, mut-p53 e HIF1α formano un complesso trascrizionale attivo sul promotore MIR30D , che porta all’espressione di miR-30d già in condizioni normossiche, ulteriormente aumentata dall’ipossia.
miR-30d regola i geni coinvolti nella via secretoria
In un primo momento, abbiamo analizzato l’impatto dell’asse mut-p53 / miR-30d sulla trasformazione cellulare in vitro. Coerentemente con i rapporti precedenti 32 , 35 , le cellule MCF10A hanno mostrato una morfogenesi acinosa normale nelle colture 3D, mentre l’espressione ectopica delle varianti mut-p53 R175H o R280K, ma non il silenziamento wt-p53 di per sé 36 , ha inibito la clearance luminale, che ricorda il fenotipo del lume pieno di carcinoma duttale in situ (Figura 2a supplementare ). In questo contesto, l’inibizione di miR-30d da parte di un vettore esca (dy-30d) 37 ha abolito il riempimento luminale (Figura 2a supplementare ), suggerendo che miR-30d media fenotipi oncogeni a valle di mut-p53.
Per identificare i processi cellulari regolati da miR-30d, abbiamo eseguito l’analisi dell’espressione genica in cellule MDA-MB-231 trasdotte stabilmente con dy-30d (di seguito denominato MDA-MB-231 / dy-30d). L’analisi dell’annotazione funzionale ha rivelato che i geni espressi in modo differenziale appartengono principalmente a categorie funzionali di trasporto di proteine, traffico vescicolare e organizzazione di Golgi (Fig. 2a ; File di dati supplementari 1 ). Gene Set Enrichment Analysis (GSEA) ha indicato che i geni regolati da miR-30d sono coinvolti nella secrezione proteica (Fig. 2b ). Abbiamo convalidato un pannello di questi obiettivi mediante qRT-PCR sulla sovraespressione di miR-30d nelle cellule MDA-MB-231. Come mostrato nella Fig. 3b supplementare , miR-30d ha migliorato l’espressione dei componenti chiave del trasporto correlato a ER (ad esempio, SEC11C, SSR1) e dei macchinari per il traffico vescicolare ER-Golgi (ad esempio, SEC23A, SEC24A, SEC24B, COPB1, ARF4, ARFGEF1, GOSR2), riducendo l’espressione dei regolatori negativi del traffico di ER-Golgi (es. ARFGAP2) e del trasporto retrogrado mediato dalla chinesina (es. KIF20A). In sintesi, i dati sull’espressione genica suggeriscono che miR-30d potrebbe modulare il traffico secretorio.
Abbiamo quindi chiesto se miR-30d influisce sulla secrezione proteica. MDA-MB-231 / dy-30d e le cellule di controllo sono state etichettate metabolicamente con amminoacidi S35 Met / Cys e le proteine secrete nel mezzo condizionato (CM) sono state analizzate mediante SDS-PAGE e autoradiografia. Come mostrato in Fig. 2c , la deplezione di miR-30d ha ridotto significativamente la secrezione proteica totale. Ciò non era dovuto alla ridotta sintesi proteica, poiché i livelli di proteine intracellulari non erano influenzati in modo apprezzabile (Figura complementare 3c ). Il knockdown di mut-p53 ha ridotto in modo simile la secrezione, che è stata salvata dalla concomitante sovraespressione di miR-30d (Fig. 2d , Figura supplementare 3d ).
Questi risultati sono stati ricapitolati nelle cellule mut-p53 R273H che esprimono MDA-MB-468 (Figura supplementare 3e ) e nelle cellule isogeniche derivate da MCF10A che esprimono mut-p53 R175H o mut-p53 R280K (Figura supplementare 3f ), indicando che diversi mutanti di p53 condividono la capacità di controllare il traffico secretorio, mentre il knockdown di wt-p53 non ha influenzato in modo significativo la secrezione proteica (Figura complementare 3f ). Infine, abbiamo verificato che il knockdown di HIF1α ha smorzato la secrezione proteica, mentre la stabilizzazione di HIF1α da parte di CoCl 2 l’ha promossa (Figura 3g supplementare ), in linea con l’osservazione che HIF1α sovraregola miR-30d.
Abbiamo quindi cercato di confermare questi risultati utilizzando un reporter per la secrezione proteica canonica 38 (ssGFP), che si localizza lungo l’intera via secretoria (Figura supplementare 4a ). In linea con i risultati di cui sopra, il knockdown di mut-p53 ha ridotto la quantità di ssGFP secreta nelle cellule MDA-MB-231, mentre la sovraespressione di miR-30d ha invertito l’effetto sia nelle colture 2D che 3D (Fig. 2e e Fig. 4b supplementare ). Risultati simili sono stati ottenuti nelle cellule DU 145 (mut-p53 P223L, V274F ), HT-29 (mut-p53 R273H ) e Mahlavu (mut-p53 R249S ) (Figura supplementare 4c – e). Allo stesso modo, la secrezione di ssGFP è stata attenuata dopo l’inattivazione di mut-p53 con APR-246 / PRIMA-1MET, o riducendo la stabilità di mut-p53 interferendo con il segnale meccanico (Figura 4f supplementare ). Come mostrato in Fig. 2f , l’inibizione di miR-30d con dy-30d ha ridotto fortemente la capacità di mut-p53 R280K di aumentare la secrezione di ssGFP nelle cellule MCF10A. Infine, silenziare mut-p53 in cellule MDA-MB-231 trasfettate con una forcina inibitrice di miR-30d (IH-30d) non ha portato a un’ulteriore riduzione significativa della secrezione di ssGFP (Figura supplementare 4g ), confermando che in queste condizioni miR -30d è un importante mediatore dell’effetto di mut-p53 sulla secrezione.
Coerentemente con l’induzione osservata di miR-30d da parte di HIF1α, il knockdown di HIF1α ha smorzato la secrezione di ssGFP, mentre l’ipossia l’ha promossa in maniera miR-30d-dipendente (Fig. 2g ).
Complessivamente, questi risultati suggeriscono che l’asse mut-p53 / HIF1α / miR-30d stimola la secrezione proteica nelle cellule tumorali.
L’asse mut-p53 / miR-30d influisce sul meccanismo di secrezione cellulare
Per caratterizzare le proteine la cui secrezione è stimolata da mut-p53 / miR-30d, abbiamo eseguito analisi di spettrometria di massa mediante tecnologia LC-MS / MS su CM raccolti da cellule di controllo e mut-p53-KD MDA-MB-231, e dalle stesse cellule che sovraesprimono miR-30d (dettagli nella Figura 4h e Metodi supplementari ).
Come mostrato in Fig. 2h , il knockdown di mut-p53 ha alterato in modo significativo il secretoma proteico delle cellule MDA-MB-231, con una regolazione sia verso l’alto che verso il basso di un gran numero di colpi; in particolare, la sovraespressione di miR-30d ha in gran parte annullato gli effetti del knockdown di mut-p53.
Abbiamo quindi confrontato i dati del secretoma mut-p53 con i dati del trascrittoma dipendente da mut-p53 e del proteoma ottenuti in precedenza nella stessa linea cellulare 30 . Ciò ha rivelato che solo il 30% circa (247/815) delle proteine secrete in modo differenziale era regolato anche a livello di trascrizione o proteina al knockdown di mut-p53 (Fig. 2i ), con una sorprendente discrepanza tra secretoma miR-30d-dipendente e trascrittoma ( solo l’11% colpisce in comune, 107/988) (Fig. 2j ). Ciò indica che l’effetto di mut-p53 / miR-30d sulla secrezione proteica dipende solo in parte dall’espressione alterata delle proteine secrete, il che implica che potrebbe interferire con il processo di secrezione.
Quindi, abbiamo analizzato la secrezione e la via del traffico nelle cellule MCF10A, silenziando wt-p53 e sovraesprimendo mut-p53 R280K o miR-30d, monitorando l’espressione del marker e la morfologia degli organelli rispetto a ER, GA, vescicole di trasporto COPI-II e microtubuli. I livelli delle proteine PDIA5, Sec24A e GM130 (marcatori per i compartimenti ER, COPI e cis- Golgi, rispettivamente) sono stati aumentati in seguito alla sovraespressione di mut-p53 R280K e miR-30d, mentre il silenziamento di wt-p53 non li ha influenzati (Fig. 5a ). L’immunofluorescenza e la microscopia confocale hanno rivelato che, mentre l’esaurimento di wt-p53 non alterava la struttura di alcun componente della via secretoria, l’espressione di mut-p53 R280K o miR-30d (Fig. 3a ) ha causato forti alterazioni della morfologia GA, con solo lievi effetti sulla morfologia ER (PDIA5), vescicole COP (Sec24A e β-COP) e microtubuli (α-tubulina). In più del 60% delle cellule che sovraesprimono miR-30d, la struttura a nastro perinucleare GA è stata sostituita da più mini-stack dispersi all’interno del citoplasma (Fig. 3a e Figura supplementare 5b ), una morfologia di seguito definita vescicolazione. Questo fenotipo è stato confermato dalla colorazione per HPA (una lectina che lega i glicani elaborati in cis -Golgi cisternae), Giantin (un marker intercisternal cross-bridge) e TGN46 (un marker trans -Golgi) (Figura supplementare 5c). Coerentemente, la ricostituzione delle immagini 3D utilizzando stack Z confocali ha rivelato un aumento da circa 10 a 60 elementi cis- Golgi per cellula in seguito alla sovraespressione di miR-30d (Figura 5d supplementare e Film 1 ).
Da notare, l’alterazione GA indotta da mut-p53 nelle cellule MCF10A è stata ripristinata dopo l’inibizione di miR-30d da parte di dy-30d (Fig. 3b ). Allo stesso modo, l’espressione ectopica delle varianti mut-p53 R175H, R273H e R280K in cellule di cancro polmonare H1299 p53-null ha indotto una vescicolazione GA che è stata abrogata inibendo miR-30d (Figura supplementare 5e ). Inoltre, le cellule MDA-MB-231 e Mahlavu hanno mostrato una morfologia GA vescicolata che è stata normalizzata al momento del knockdown di mut-p53 o del trattamento con PRIMA-1MET, e ripristinata dall’introduzione di miR-30d (Fig. 3c e Figura 5f supplementare ).
Questi risultati confermano che mut-p53 modifica la morfologia GA e miR-30d è uno dei principali mediatori di questa attività. Coerentemente con la regolazione osservata di miR-30d da HIF1α, l’attivazione di HIF1α da ipossia o il trattamento con CoCl 2 ha causato una modifica simile della struttura GA che è stata ridotta dall’inibizione di miR-30d (Figura complementare 5g ).
Per caratterizzare le alterazioni GA indotte dall’asse mut-p53 / miR-30d, abbiamo eseguito analisi ultrastrutturali mediante microscopia elettronica a luce correlativa (CLEM) in cellule MCF10A. Mentre le cellule di controllo mostravano la canonica ultrastruttura GA, le cellule con sovraesprimono miR-30d mostravano GA tubulo-vescicolate, caratterizzate da cisterne strette con pori larghi, connessioni intercisternali, invaginazioni di membrana e gonfiore delle cisterne (Fig. 3d ). È stato rilevato anche un aumento del numero di vescicole COPI. L’analisi CLEM ha indicato che l’esaurimento di wt-p53 non ha alterato la struttura GA, mentre la sovraespressione di mut-p53 R280K ha causato la comparsa di cisterne parzialmente tubulate (Fig. 3d). Da notare, l’inibizione di miR-30d ha ripristinato la normale struttura degli stack GA nelle cellule con sovraesprimono mut-p53 (Fig. 3d ), confermando la relazione epistatica. La ricostituzione di singole cisterne è mostrata nella figura supplementare 5h-l .
Alterazioni della struttura GA simili a quelle indotte da mut-p53 / miR-30d sono state precedentemente segnalate per accelerare la diffusione di proteine solubili da cis a trans Golgi, lasciando inalterato o riducendo il traffico di carichi non diffusibili comprese le proteine di membrana 39 , 40 . Inoltre, l’aumento osservato delle vescicole COPI suggerisce che potrebbe verificarsi un maggiore recupero delle proteine residenti ER e Golgi per mantenere la corretta distribuzione intracisterna degli enzimi Golgi. Per analizzare le alterazioni della cinetica di trasporto delle proteine indotte da mut-p53 / miR-30d abbiamo utilizzato il sistema reporter RUSH, che permette di sincronizzare l’uscita ER delle proteine espresse ectopicamente 41. Abbiamo trasfettato come reporter l’α-mannosidasi II (MannII) fusa con il dominio di legame della streptavidina insieme a un costrutto di streptavidina-KDEL come gancio per la ritenzione di ER. Mannii permette di seguire il traffico da ER a mediale-trans Golgi 42 , 43 . Come mostrato in Fig. 3e , la sovraespressione di miR-30d è associata a una più rapida localizzazione del Golgi di MannII (20 minuti dopo la sincronizzazione contro 50 minuti nelle cellule di controllo).
Questi risultati dimostrano che mut-p53, tramite miR-30d, modifica il meccanismo secretorio inducendo la tubulo-vescicolazione dell’apparato di Golgi e aumenta il tasso di traffico.
miR-30d regola gli obiettivi coinvolti nella via secretoria
Abbiamo cercato di identificare target miR-30d candidati che potrebbero mediare i fenotipi osservati. Avendo dimostrato che l’espressione di miR-30d è indotta da mut-p53 e HIF1α, abbiamo utilizzato i dati trascrittomici disponibili per confrontare tre elenchi di geni: (i) geni sottoregolati da mut-p53 (sip53 UP, cioè geni sovraregolati da mut-p53 KD in Cellule MDA-MB-231 30 , (ii) geni sottoregolati da HIF1α 33 (siHIF1α UP) e (iii) geni sottoregolati da miR-30d (dy-30d UP, ovvero geni sovraregolati da dy-30d in MDA-MB- 231 cellule) .L’intersezione di questi insiemi ha restituito 118 geni comunemente regolati da mut-p53 / HIF1α / miR-30d; dieci di questi mRNA sono predetti target di miR-30d in silico ( www.targetscan.org ) (Fig. 4a). La convalida mediante RT-qPCR ha confermato che mut-p53 reprime AP2A1, DGKZ, IQCG, PPP3CB e VPS26B attraverso miR-30d (Fig. 4b e Fig. 6a supplementare ). È interessante notare che questi geni sono stati associati al traffico vescicolare e ai processi di riciclaggio. Abbiamo analizzato la capacità di miR-30d di sottoregolare direttamente questi mRNA mediante saggi reporter 3’UTR-luciferasi (Fig. 4c – d , Figura supplementare 5b ). Abbiamo osservato una riduzione dell’attività del reporter solo per i costrutti DGKZ e VPS26B, che è stata prevenuta introducendo mutazioni mirate nei siti di legame previsti per miR-30d, suggerendo che DGKZ e VPS26B sono bersagli diretti di miR-30d (Fig. 4d). Coerentemente, le proteine endogene DGKZ e VPS26B sono aumentate in seguito alla deplezione di mut-p53 nelle cellule MDA-MB-231, mentre la sovraespressione di miR-30d ha invertito questo effetto (Figura 6c supplementare ). Allo stesso modo, le condizioni ipossiche hanno ridotto i trascritti DGKZ e VPS26B, mentre il knockdown di HIF1α li ha aumentati (Figura supplementare 6d ).
DGKZ è un enzima appartenente alla famiglia dei diacilgliceroli chinasi 44 , mentre VPS26B è un componente del complesso retromer core, che media il riciclo delle proteine durante lo smistamento endosomiale 45 , 46 . VPS26B e il suo paralogo VPS26A rappresentano subunità che si escludono a vicenda che definiscono complessi retromer distinti 47 . Da notare, mut-p53 e miR-30d regolano specificamente l’espressione di VPS26B, pur non influenzando VPS26A (Figura 6e supplementare ).
Successivamente abbiamo studiato il ruolo di DGKZ e VPS26B nella morfologia GA. Come mostrato in Fig. 4e , la sottoregolazione di DGKZ o VPS26B da parte di RNAi ha indotto la vescicolazione GA nelle cellule MCF10A, imitando la sovraespressione di miR-30d. Abbiamo quindi analizzato la secrezione proteica mediante etichettatura metabolica: l’esaurimento di DGKZ o VPS26B nelle cellule MCF10A ha determinato un aumento significativo della secrezione proteica totale, in modo simile alla sovraespressione di miR-30d (Fig. 4f , Figura supplementare 6f ).
Catalizzando la conversione del diacilglicerolo lipidico di membrana (DAG) in acido fosfatidico, DGKZ riduce i livelli di DAG alle membrane 44 . La concentrazione locale di DAG regola la tubulo-vescicolazione 48 del Golgi e promuove il traffico da trans- Golgi alla membrana plasmatica tramite l’attivazione della chinasi PKD 49 , 50 residente nel Golgi . Abbiamo quindi ipotizzato che la downregulation di DGKZ da parte di miR-30d possa portare all’accumulo di DAG alle membrane di Golgi che inducono l’attivazione PKD locale. Abbiamo testato questa possibilità utilizzando una sonda fluorescente costituita dal dominio di legame DAG di PKCγ fuso a GFP . Nelle cellule MDA-MB-231, il knockdown di mut-p53 ha ridotto i livelli di DAG a livello cis e transGolgi, mentre la sovraespressione concomitante di miR-30d ha salvato l’accumulo di DAG . Abbiamo quindi monitorato l’attivazione di PKD1 al knockdown di mut-p53, osservando una riduzione della forma fosforilata attiva di PKD1 sia nei lisati cellulari totali che specificamente alle membrane di Golgi come indicato dall’immunofluorescenza e dall’imaging confocale, mentre la sovraespressione di miR-30d o il knockdown di DGKZ hanno invertito questo effetto . È quindi concepibile che l’accumulo di DAG e la conseguente attivazione di PKD contribuiscano alla capacità di mut-p53 / miR-30d di aumentare la secrezione.
MiR-30d è stato precedentemente segnalato per ridurre l’espressione della transferasi Golgi GalNAc GALNT7, influenzando la O-glicosilazione e promuovendo l’invasione e la metastasi delle cellule di melanoma . Abbiamo confermato che miR-30d riduceva l’espressione di GALNT7 anche nelle cellule MDA-MB-231 . Tuttavia, l’esaurimento di GALNT7 nelle cellule MCF10A non ha causato né vescicolazione GA , né una maggiore secrezione di ssGFP, suggerendo che la sua sottoregolazione non contribuisce all’alterazione GA da parte di miR-30d.
Complessivamente, questi risultati identificano DGKZ e VPS26B come bersagli diretti dell’asse mut-p53 / miR-30d, la cui inibizione contribuisce alla vescicolazione di GA e all’aumento della secrezione. Inoltre, questi dati suggeriscono che l’inibizione di DGKZ da parte di miR-30d influenza la morfologia e la funzione di GA alterando la segnalazione dipendente da DAG.
È interessante notare che anche gli effetti indiretti del miR-30d, in particolare la stabilizzazione dei microtubuli (come giudicato dalla colorazione per la tubulina acetilata , possono promuovere la secrezione. Infatti, l’agente stabilizzante dei microtubuli Taxol, che aumenta la vescicolazione del Golgi e la secrezione proteica , salva parzialmente la secrezione di ssGFP in seguito all’inibizione di miR-30d nelle cellule MDA-MB-231 .
Impatti del secretoma Mut-p53 / miR-30d sul microambiente tumorale
Abbiamo quindi studiato la rilevanza funzionale della secrezione alterata da mut-p53 / miR-30d. L’analisi bioinformatica del secretoma mut-p53 / miR-30d ha rivelato l’arricchimento della composizione e del rimodellamento dell’ECM, l’adesione cellula-ECM e l’adesione cellula-cellula, l’angiogenesi e le categorie funzionali di migrazione.
Questo ci ha spinto a esplorare se la riprogrammazione dei secretomi potrebbe influenzare la diafonia delle cellule tumorali con il loro microambiente. In particolare, la deposizione e il rimodellamento di ECM alterati aumenta la rigidità stromale e influisce sui segnali meccanici, alterando l’attività dei CAF e di altre cellule che popolano la TME 4 . L’analisi immunoblot di MDA-MB-231 CM ha evidenziato che il knockdown di mut-p53 ha ridotto i componenti ECM secreti tra cui fibronectina, laminina V e laminina B1, mentre la sovraespressione di miR-30d li ha aumentati . Di conseguenza, utilizzando la microscopia a forza atomica abbiamo scoperto che il knockdown di mut-p53 nelle cellule MDA-MB-231 ha ridotto la rigidità dell’ECM (0,15 kPa contro 0,25 kPa), mentre la sovraespressione di miR-30d ha indotto una ECM più rigida (0,30 kPA).
Successivamente, abbiamo valutato gli effetti paracrini del secretoma mut-p53 / miR-30d sulle cellule tumorali e stromali, compresi i fibroblasti e le cellule endoteliali. Per valutare l’impatto sulla migrazione delle cellule tumorali, le cellule tumorali polmonari H1299 sono state trattate con CM raccolti da cellule H1299 o MDA-MB-231. Il CM delle cellule MDA-MB-231 ha aumentato la migrazione delle cellule H1299 più di due volte, un effetto significativamente ridotto all’esaurimento di mut-p53 nelle cellule donatrici. La sovraespressione di miR-30d era sufficiente per ripristinare una secrezione pro-migratoria nelle cellule MDA-MB-231 mut-p53-KD . Allo stesso modo, l’inibizione di miR-30d ha abolito l’effetto pro-migratorio di MDA-MB-231 CM sulle cellule H1299 . Da notare, questa proprietà si basa sulla componente proteica del secretoma, poiché è stata abolita dalla denaturazione termica.
Successivamente, abbiamo analizzato l’impatto del secretoma mut-p53 / miR-30d sulle cellule endoteliali e sui fibroblasti. Mut-p53 promuove direttamente la trascrizione di VEGFA e, coerentemente con l’analisi del secretoma, mut-p53 aumenta la secrezione di questo fattore proangiogenico nelle cellule MDA-MB-231 anche tramite miR-30d. Abbiamo valutato l’effetto del secretoma mut-p53 / miR-30d sulle cellule endoteliali eseguendo analisi di angiogenesi e permeabilità vascolare in vitro utilizzando cellule endoteliali della vena ombelicale umana (HUVEC). Il precondizionamento con MDA-MB-231 CM ha aumentato sia il numero di anelli chiusi HUVEC, sia la permeabilità al destrano dei monostrati HUVEC, indicando un aumento dell’angiogenesi e della perdita endoteliale. Entrambi gli effetti sono stati ridotti dal knockdown di mut-p53 e recuperati dalla sovraespressione di miR-30d nelle cellule mut-p53-KD ).
Abbiamo quindi valutato l’effetto del secretoma mut-p53 / miR-30d sull’attivazione di fibroblasti umani di tipo normale BJ e Wi-38 nei test di guarigione delle ferite. Il precondizionamento con CM ottenuto da cellule MDA-MB-231 o MDA-MB-468 ha migliorato la migrazione dei fibroblasti e la chiusura della ferita; questi effetti sono stati attenuati silenziando mut-p53 nelle cellule donatrici e sono stati recuperati dalla sovraespressione di miR-30d Inoltre, il precondizionamento delle cellule BJ con CM da cellule MDA-MB-231 cresciute sotto ipossia ha ulteriormente migliorato la migrazione dei fibroblasti e la chiusura della ferita, e questi effetti sono stati ridotti dall’inibizione di miR-30d nelle cellule del donatore . È importante sottolineare che l’inibizione della secrezione nelle cellule donatrici che esprimono mut-p53 mediante il trattamento con BFA ha abolito il loro effetto pro-migratorio. Abbiamo anche osservato l’induzione di marker attivi di fibroblasti associati al cancro (CAF) tra cui fibronectina, α-SMA, HIF e YAP in fibroblasti Wi-38 trattati con MDA-MB-231 CM, in un mut-p53 / miR-30d- modo dipendente, indicando che questo asse causa l’attivazione funzionale e metabolica dei CAF. Infine, abbiamo verificato se questo effetto di miR-30d richiedesse una sottoregolazione di DGKZ e VPS26B. L’inibizione di miR-30d nelle cellule MDA-MB-231 ha aumentato l’espressione di DGKZ e VPS26B e contemporaneamente ha ridotto la stimolazione paracrina della migrazione dei fibroblasti. In questo contesto, silenziare DGKZ o VPS26B nelle cellule MDA-MB-231 / miR-30d-dy ha parzialmente ripristinato l’induzione della migrazione di CAF e la chiusura della ferita , confermando che miR-30d promuove il reclutamento di CAF almeno in parte inibendo questi bersagli.
Questi risultati suggeriscono che il secretoma mut-p53 / miR-30d potrebbe agire localmente in modo paracrino sulle popolazioni di cellule tumorali e stromali, sia inducendo la deposizione e il rimodellamento dell’ECM sia tramite la segnalazione di fattori solubili secreti.
miR-30d migliora la tumorigenesi e le metastasi in vivo
Per studiare l’impatto del secretoma dipendente da miR-30d sulla crescita del tumore e sulle metastasi in vivo, topi immunodeficienti sono stati iniettati ortotopicamente con cellule MDA-MB-231 che esprimono luciferasi (MDA-MB-231-LUC), trasdotte stabilmente con controllo o costrutto dy-30d. L’inibizione di miR-30d ha ritardato significativamente la crescita del tumore per un periodo di 4 settimane (Fig. 6a ).